CD47开发火热,差异化布局正在开始
- 2021-11-02 11:09
- 作者:陈倩
- 来源:中国食品药品网
PD-1/L1抑制剂后,CD47成为另一个免疫检查点抑制剂中的热门靶点,不仅在尚未被PD-1/L1抑制剂颠覆的血液肿瘤治疗格局中显示出疗效,同时这一控制先天免疫的通路,在理想的状态下,希望能实现与现有适应性免疫治疗进行联合的方式。全球CD47-SIRPα通路开发处于临床阶段的药物已超过30个,不仅作为单药,还有希望能成为新的免疫联合治疗支柱。
CD47-SIRPα通路靶向药开发火热
CD47作为天然免疫重要的“免疫检查点”分子,对细胞的迁移、粘附、增殖和凋亡都能发挥作用。在肿瘤细胞表面广泛高表达,如卵巢癌、胃癌和非小细胞肺癌,可与巨噬细胞表面的信号调节蛋白α(SIRPα)结合并发出“别吃我”信号以逃避免疫监视。SIRPα的表达相对没有CD47那么广泛,主要存在于骨髓细胞上,如巨噬细胞和骨髓树突状细胞。除SIRPα外,CD47还会与整合素、血小板反应蛋白-1结合。
靶向CD47-SIRPα信号转导的策略和目标是阻止两者的结合,停止癌细胞向巨噬细胞发出“不要吃我”的信号。虽然癌细胞通常有一些现有的前吞噬信号,但阻断CD47和SIRPα结合不足以触发癌细胞的吞噬作用。相反,需要通过用额外的“吃我”信号标记癌细胞来增强前吞噬信号。目前还没有一款针对CD47-SIRPα信号转导通路的药物上市。
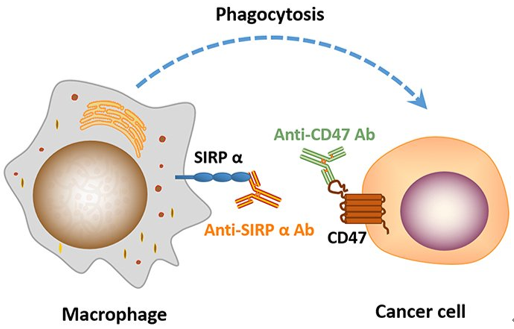
图1 用抗CD47或SIRPɑ抗体可以作为诱导巨噬细胞吞噬肿瘤细胞
最早进入临床研发的是CD47单抗。当CD47单抗杀死肿瘤细胞时,它们不可避免地引起红细胞凝集,并继发引起红细胞的裂解,贫血和血小板减少症已成为剂量限制性毒性因素,CD47单抗药物在到达肿瘤细胞之前就会被红细胞耗尽。目前Forty Seven、新基和Surface Oncology等公司的做法是用IgG4连接Fc端,而不是能引发强ADCC和CDC效应的IgG1型抗体。这种策略虽然能降低抗体对红细胞和血小板的影响,但用IgG4代替IgG1会大大削弱CD47抗体药物对肿瘤细胞的杀伤能力,这可能也是导致Celgene终止CC-90002临床试验的原因之一。
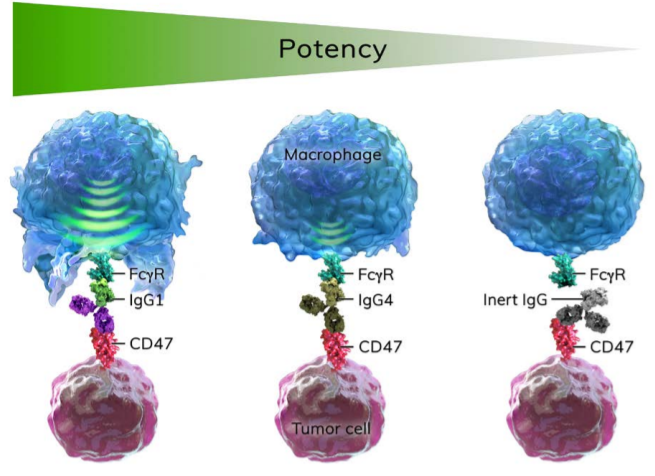
图2 单药诱导巨噬细胞对肿瘤的杀伤力与IgG亚类的选择有关
另有一种方式还有完全摒弃CD47抗体的强效ADCC效应,只利用CD47-SIRPα本身的生物学效应来释放巨噬细胞的抗肿瘤潜力。一些公司也采用新的方法,例如ALX Oncology开发的ALX148使用了没有生物活性的Fc端;AO-176采用的是IgG2型单抗,可以在酸性微环境(低PH)中更有效地结合肿瘤,诱导损伤诱导分子模式(damp)并对肿瘤直接杀伤。但在这种情况下,CD47药物必须与其他药物联合使用,尤其是ADCC效应能决定巨噬细胞和自然杀伤细胞吞噬的抗肿瘤药物,或与PD-1/PD- L1抑制剂能系统性调节免疫的药物,以增加先天性和适应性肿瘤免疫反应以及细胞因子的释放。目前处于临床阶段的CD47抗体/融合蛋白药物主要针对血液肿瘤,也有部分处于早期临床阶段的项目开始在实体瘤进行探索。
靶向SIRPα以阻断CD47-SIRPα检查点的主要优点是SIRPα的组织分布有限,且不在红细胞上表达,这种狭窄的表达谱减少了与CD47抗体相关的潜在抗原沉默问题,这意味着可以降低实现最大受体占用所需的剂量,还可能会减少相关贫血等毒性。然而,由于SIRPα主要在神经元和骨髓细胞中表达,所以SIRPα单抗需要有一个失活的Fc区来提高安全性,但这也限制了使用SIRPα单抗药物作为单一疗法的可能性。
Trillium和ALX Oncology引领了SIRPα融合蛋白药物的研发,SIRPα-Fc融合蛋白由SIRPα的胞外域与IgG Fc片段融合而成,与Fc片段融合有几个优势,首先能延长药物半衰期和提高分子稳定性;其次能保留Fc段介导的效应功能。Trillium同时开发了两款SIRPα融合蛋白,分别为IgG1亚型和IgG4亚型。ALX Oncology的ALX148则采用IgG4亚型。
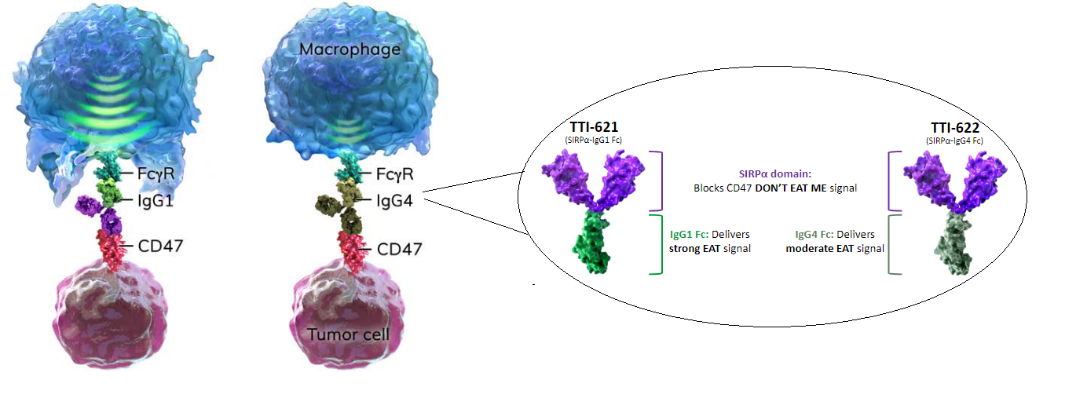
图3 Trillium同时开发两款不同IgG亚型的SIRPα融合蛋白
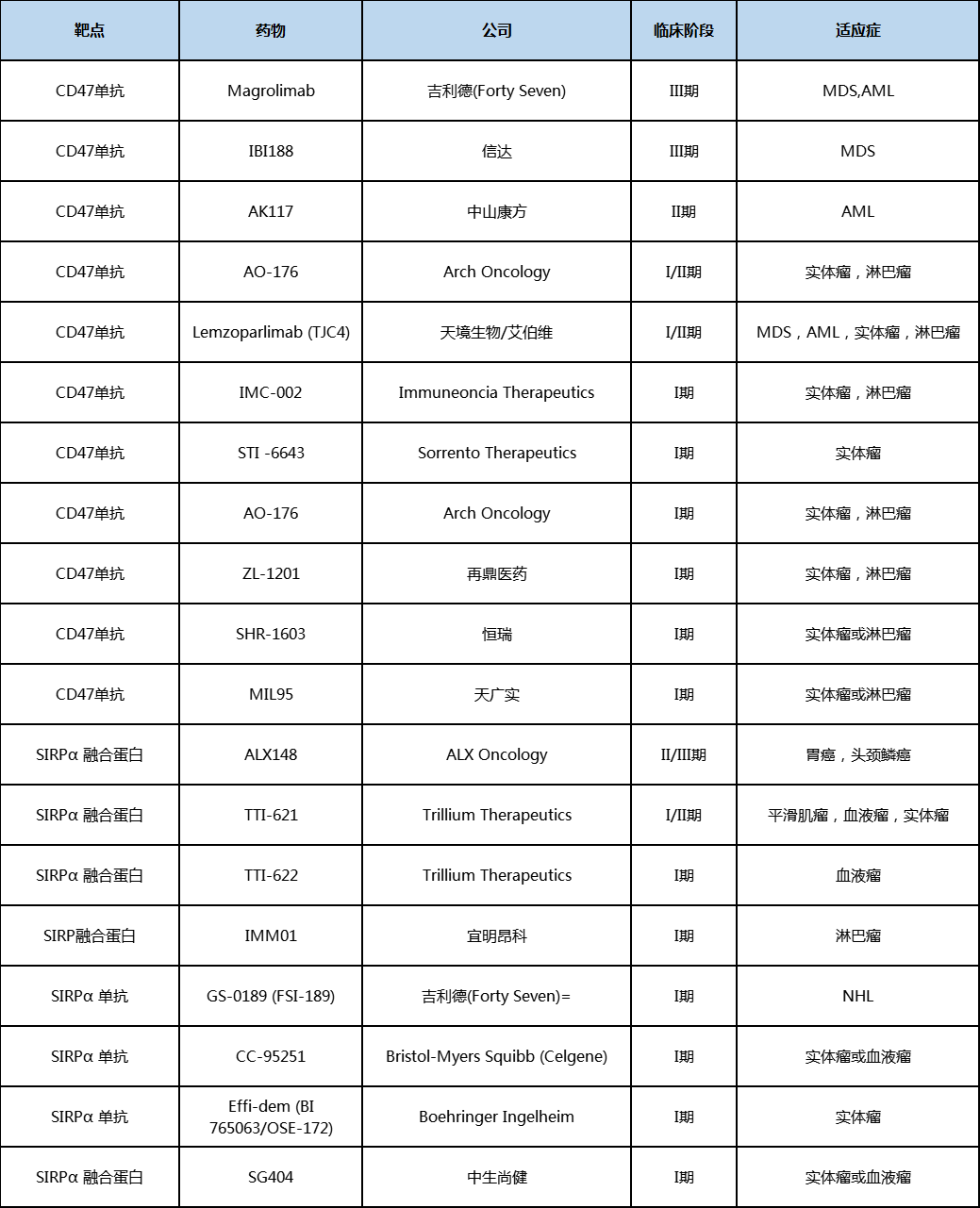
表1 临床阶段CD47和SIRPα抗体/融合蛋白药物
管线拥挤中的差异化竞争
CD47领域看似很拥挤,但因为开发技术的差异,使得他们在不同适应症的开发也呈差异化。
虽然吉利德的magrolimab明显领先于其竞争对手,并且最有可能成为市场上第一个CD47抗体。通过1b期临床试验的初步疗效数据获得了美国FDA的快速通道资格认定,对于未接受过治疗的高危骨髓增生异常综合征(MDS)患者和急性髓系白血病(AML)患者,magrolimab治疗的总缓解率(ORR)分别为100%和64%,目前正在进行magrolimab+阿扎胞苷用于AML一线治疗的III期临床试验,为已经陷入治疗瓶颈10年的AML带来治疗机会。
2021年8月,辉瑞宣布以22.6亿美元收购Trillium Therapeutics公司引起不少关注,收购获得了两款潜在同类最佳的SIRPα-Fc融合蛋白TTI-621和TTI-622,两个产品均具有单一疗法活性。在TTI-621作为单一疗法以及与利妥昔单抗(抗 CD20)或Nivolumab(抗 PD-1)联合治疗复发性或难治性血液系统恶性肿瘤的I期临床试验中,对于弥漫性大B细胞淋巴瘤(DLBCL)患者,TTI-621作为单一疗法的ORR为29% (2/7),TTI-621+利妥昔单抗的ORR为 21% (5/24)。由于样本量相对较小很难得出结论,但CD47+CD20似乎并没有改善ORR。同时,TTI-622单药用于实体瘤和血液瘤的临床试验正在进行中,中期数据显示TTI-622耐受性良好,最大剂量已爬到18mg/kg,1b/2期将选择从8mg/kg开始。由于 TTI-622的最大剂量远大于TTI-621的最大剂量,有可能与TTI-622能达到更高的受体占优率有关。
值得注意的是,虽然magrolimab和ALX148单药治疗疗效不佳,但当与利妥昔单抗联合治疗复发性或难治性CD20阳性B细胞非霍奇金淋巴瘤时,ORR分别为50%和70%。
AXL公司的SIRPα-Fc融合蛋白ALX148,是最早开始联用并开始在实体瘤探索的药物。在去年ASCO上公布了ALX148的I期临床试验结果,在单药爬坡中显示ALX148耐受性良好,在剂量≥3mg/kg时达到接近完全受体占优,但单药活性小,24名可评估患者中有6名对稳定疾病有最佳反应。因此,未来的工作重点是开发用于联合治疗的ALX148,10mg/kg的ALX148与Pembrolizumab/Trastuzumab联合用于头颈部鳞状细胞癌(HNSCC)、HER2阳性胃癌和非小细胞肺癌(NSCLC)的试验中。

图4 ALX148联合治疗I期临床试验结果
初步结果显示,在头颈部鳞状细胞癌(HNSCC)队列中,10名CPI初治二线治疗患者中ORR为40%(n=4),此前pembrolizumab作为单药治疗HNSCC仅有15%的ORR;在HER2阳性胃癌队列中,当与trastuzumab联合使用时,19名患者中有4 名部分应答。当与trastuzumab、ramucirumab、紫杉醇联用时,18名患者中有13名有应答。而此前曲妥珠单抗联合紫杉醇的应答率为33%,而雷莫芦单抗联合紫杉醇的应答率为28%。10mg/kg的ALX148与派姆单抗联合作为NSCLC的二线或后续治疗,20名患者有1名获得PR。尽管ALX148组合的样本量非常小,但这个结果令人兴奋。目前正在采用类似策略的还有天境生物的lemzoparlimab单药应答率低,但在与阿扎胞苷联合的AML/MD组合试验中观察到了令人鼓舞的临床疗效信号。
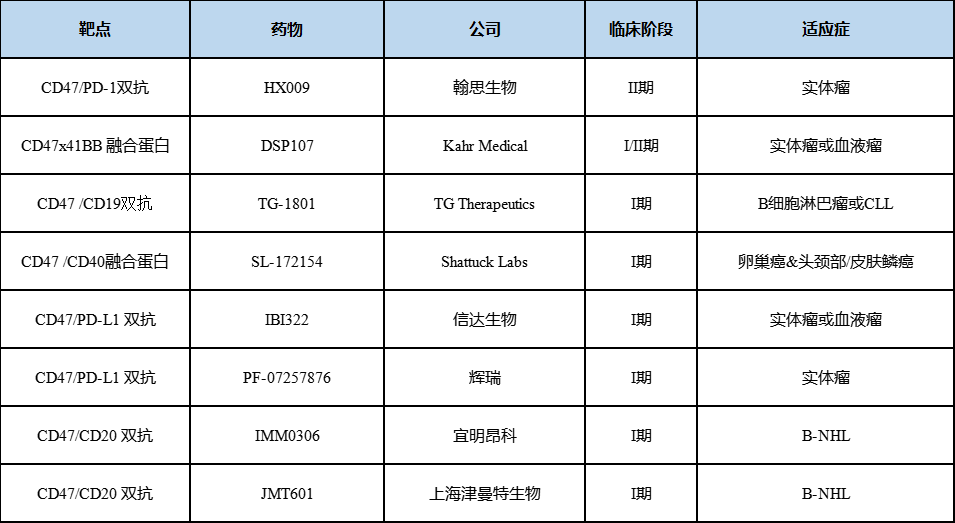
目前也有采取双抗策略的,双特异性抗CD47包括双特异性抗体和双特异性融合蛋白。共同靶向CD47和其他肿瘤特异性抗原可能会提高CD47靶向抗体的结合特异性,从而提高安全性和有效性。
表2 临床阶段CD47双抗药物
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐













