每周医药看点(11月25日—12月1日)
- 2024-12-04 14:12
- 作者:张可欣
- 来源:中国食品药品网
中国食品药品网讯 国家药监局、海关总署发布关于增设云南省勐康、磨憨口岸为药材进口边境口岸的公告;国家医疗保障局办公室印发《短缺药品价格的风险管理操作指引》,国家药监局发布《中药生产监督管理专门规定(征求意见稿)》……11月25日—12月1日,医药行业的这些动态值得关注。
行业·政策动态
1.国家卫生健康委等7部门制定印发《关于进一步推进医疗机构检查检验结果互认的指导意见》(以下简称《指导原则》)。《指导原则》指出,到2025年底,各紧密型医联体(含城市医疗集团和县域医共体)实现医联体内医疗机构间全部项目互认,各地市域内医疗机构间互认项目超过200项。到2027年底,各省域内医疗机构间互认项目超过300项;京津冀、长三角、成渝等区域内医疗机构互认项目数超过200项。到2030年,全国互认工作机制进一步健全完善,检查检验同质化水平进一步提高,结果互通共享体系基本建立,基本实现常见检查检验结果跨区域、跨医疗机构共享互认。
2.国家药监局、海关总署发布关于增设云南省勐康、磨憨口岸为药材进口边境口岸的公告。自2024年11月29日起,中药材可经由勐康口岸、磨憨口岸(含磨憨铁路口岸)进口。所进口药材应符合《进口药材管理办法》等有关规定。
3.国家医疗保障局办公室印发《短缺药品价格的风险管理操作指引》(以下简称《操作指引》)。《操作指引》共分为总则、价格风险防范、价格风险发现、价格风险应对、优化服务管理、附则六部分共31条。
4.国家药监局发布《中药生产监督管理专门规定(征求意见稿)》,并公开征求意见。征求意见截止时间为2024年12月25日。
5.国家药监局就《医药代表管理办法(征求意见稿)》(以下简称《征求意见稿》)公开征求意见。相比现行《医药代表备案管理办法(试行)》,《征求意见稿》对医药代表的定义及工作内容略作调整,夯实药品上市许可持有人管理责任,增加对医疗卫生机构及其工作人员的管理规定,为多方制定完善禁止行为清单,进一步厘清医药代表与药品销售人员的边界。
6.国家药监局药审中心(CDE)发布公告,将ALXN1850注射液[申报单位阿斯利康全球研发(中国)有限公司]、RAG-17注射液[申报单位中美瑞康核酸技术(南通)研究院有限公司]、VGR-R01(申报单位上海天泽云泰生物医药有限公司)纳入“以患者为中心的罕见疾病药物研发试点工作计划”(“关爱计划”)。
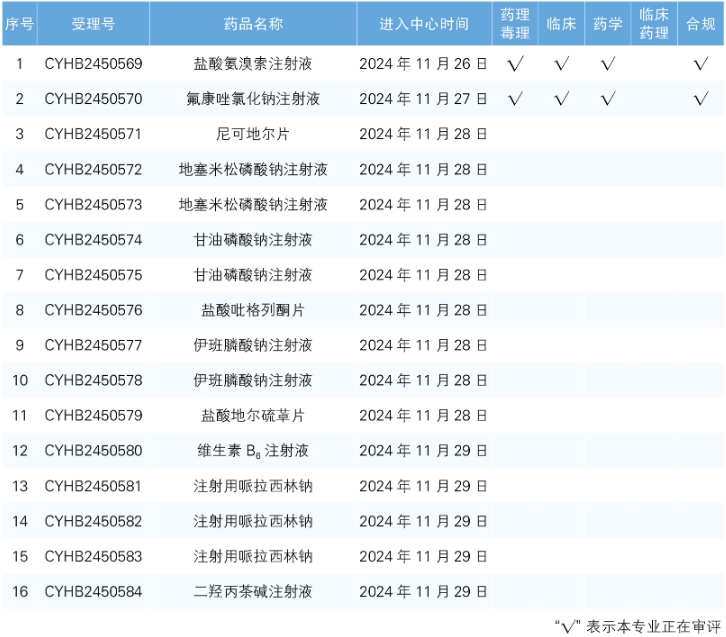
7.CDE网站公示16个仿制药一致性评价任务,涉及盐酸氨溴索注射液等药品(截至12月1日)。
产品研发·上市信息
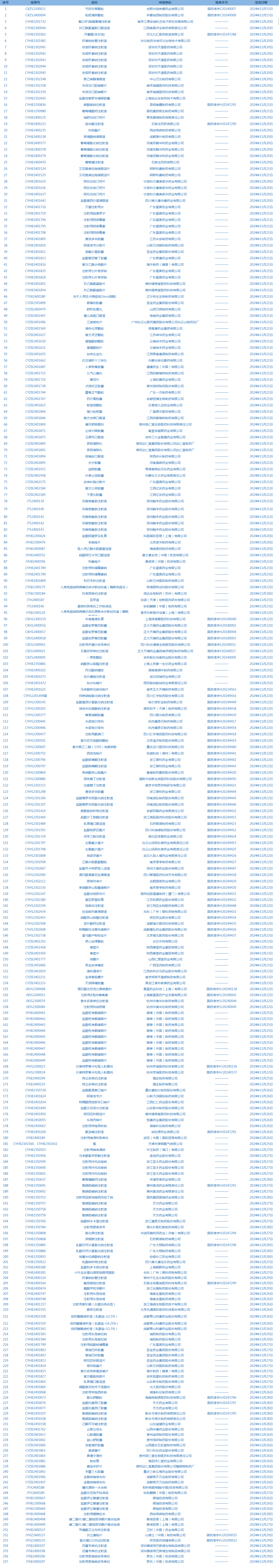
1.国家药监局发布5期药品批准证明文件送达信息,共包括257个受理号,涉及合肥华润神鹿药业有限公司等企业(截至12月1日)。
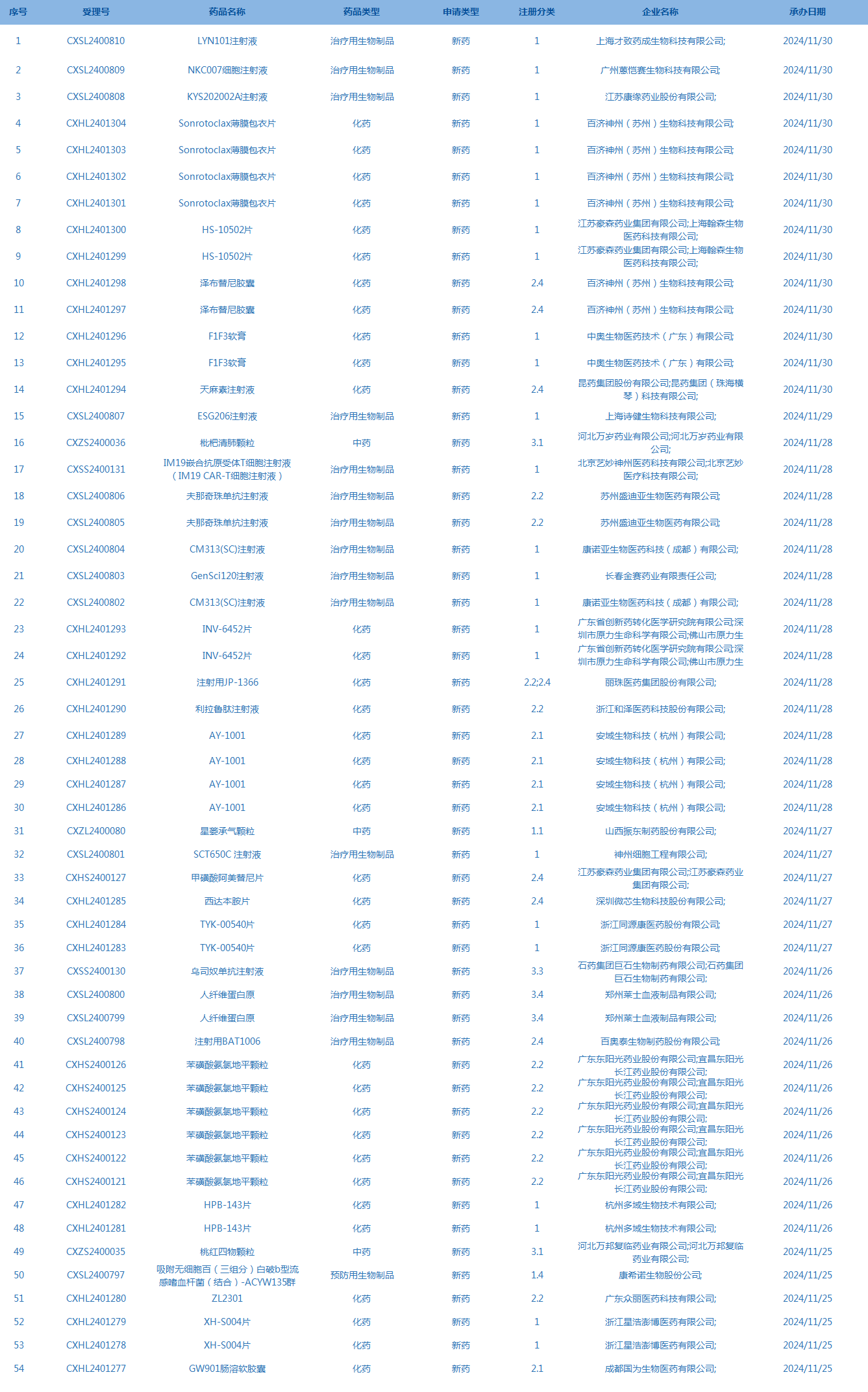
2.CDE承办受理54个新药上市申请,包括LYN101注射液等(截至12月1日)。
3.以岭药业发布公告称,其全资子公司以岭万洲国际制药有限公司向美国FDA申报的辛伐他汀片的新药简略申请(ANDA)已获得批准。
4.新华制药发布公告称,收到美国FDA核准签发的碳酸司维拉姆原料药注册批准函。
5.汇宇制药发布公告称,其全资子公司Seacross Pharmaceuticals Ltd.于近日收到英国药品和健康产品管理局核准签发的注射用伏立康唑、氟维司群注射液的上市许可。
医药企业观察
1.丹诺医药宣布与远大生命科学集团就治疗幽门螺杆菌感染抗菌新药产品TNP-2198签署独家商业合作协议,授权远大生命科学集团全资子公司杭州远大生物制药有限公司(以下简称杭州远大)作为TNP-2198在中国的独家商业化推广服务商。根据协议,杭州远大将向丹诺医药支付首付款、商业化里程碑付款以及销售里程碑付款,合计付款金额最高不超过7.75亿元。丹诺医药将作为上市许可持有人负责TNP-2198的后续临床开发、上市注册等工作,同时向杭州远大支付市场推广服务费。
2.三生制药宣布,旗下沈阳三生制药有限责任公司(以下简称沈阳三生)与广东东阳光药业股份有限公司(以下简称东阳光药)及其子公司宜昌东阳光长江药业股份有限公司就苯磺酸克立福替尼达成合作协议。根据协议,沈阳三生将获得东阳光药自主研发的苯磺酸克立福替尼在中国关于特定适应证的独家商业化权利。沈阳三生将向东阳光药支付首付款以及研发及销售里程碑付款。东阳光药将继续负责克立福替尼的研发、注册和生产。
3.九源基因近日正式在香港证券交易所主板挂牌上市。据了解,九源基因创立于1993年,拥有逾30年生物药品及医疗器械研发、生产及商业化经验,专注于骨科、代谢疾病、肿瘤及血液四大治疗领域,已建立六个产品开发平台,能持续开发及推进管线产品。
4.南京英派药业有限公司(以下简称英派药业)宣布于近日顺利完成2.5亿元人民币D++轮融资。本轮融资由全球知名产业投资机构和知名保险基金共同投资。融资资金将支持英派药业核心产品塞纳帕利的商业化,及包含PARP1选择性抑制剂在内的多个化合物的全球临床开发,同时用于加速多个早期项目的研发。
药品集中采购
1.国家医保局召开新闻发布会,宣布《国家基本医疗保险、工伤保险和生育保险药品目录(2024年)》(以下简称医保目录)调整工作全面完成。通过本次调整,共有91种药品新增进入医保目录,另有43种原目录内药品被调出目录。新增的91种药品中有90个为5年内新上市品种,其中38个是“全球新”的创新药。
2.重庆市医保局公布《重庆市“三进”集采药品清单》,共有681个通用名、1867个品规纳入“三进”清单。
3.三明采购联盟办公室发布《三明采购联盟药品和医用耗材集中带量采购公告(第1号)》。本次采购联盟包括三明采购联盟成员、河北省、辽宁省、黑龙江省、安徽省、江西省、广西壮族自治区、海南省、甘肃省、青海省,纳入集采的药品为19种,耗材3种。企业报名时间为2024年11月27日9:00—11月29日17:00。(本报记者张可欣整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:周雨同)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐