11月份美国Clinicaltrial数据库临床试验数据显示—— 正大天晴新开临床试验数量位列全球第八
- 2024-12-26 13:47
- 作者:陈宇哲
- 来源:中国医药报
根据美国Clinicaltrial数据库数据,2024年11月份,全球新增由企业资本主导的临床试验738项,数量较10月份上升0.68%,但低于2023年同期水平,同比下降1.86%。值得关注的是,中国药企正大天晴进入新开临床试验数量排名前十的企业榜单,排在第八位。
新开临床试验整体情况
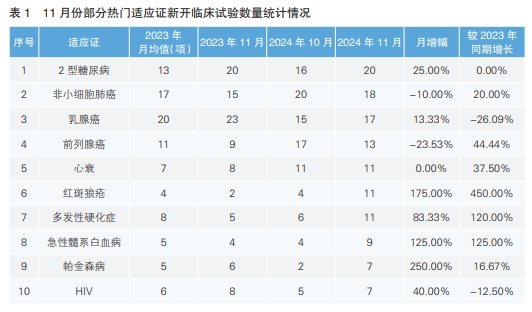
从11月份新增临床试验热门适应证来看,2型糖尿病为最热门的研发领域,新开临床试验20项,环比增长25.00%,与去年11月份数量一致;其次为非小细胞肺癌,新开临床试验数量环比下降10%,但同比上升20%。值得注意的是,11月份新开临床试验数量增幅超过两倍的热门适应证为帕金森病,由10月份的2项上升为7项,环比增长250%。相较于去年同期,新开临床试验数量上升幅度最大的适应证为红斑狼疮,由去年同期的2项增长为11项,同比增长450%(详见表1)。
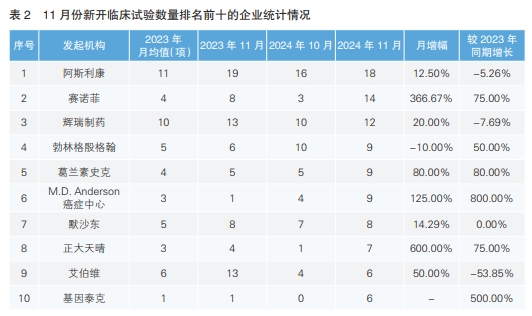
对新增临床试验的发起单位进行统计后发现,11月份发起临床试验最多的机构为阿斯利康,新开临床试验18项,环比上升12.50%,但同比下降了5.26%;其次为赛诺菲,新开临床试验数量环比上升了366.67%,同比增长75.00%。新开临床试验数量增幅最大的发起单位为正大天晴,环比增长了六倍,同比增长了75%(详见表2)。
对临床试验的申请国家和地区进行统计后发现,11月份美国仍为临床试验开展最为主要的国家,新开临床试验217项,数量相较于10月份下降了13.20%。其次是中国,新开设临床试验82项,相较于10月份上升了7.89%。新开临床试验数量月增长幅度最大的国家为德国,新开设临床试验由10月份的10项增长为12项,上升20.00%;月降低幅度最大的为澳大利亚,由10月份的26项降低为14项,环比下降了8.33%。
正大天晴发起七项临床试验
11月份正大天晴发起的临床试验有7项,包括1项Ⅲ期临床试验,3项Ⅱ期临床试验和3项Ⅰ期临床试验。
Ⅲ期临床试验(NCT06682169)的对象为罗伐昔替尼(TQ05105),适应证为移植物抗宿主病。罗伐昔替尼是正大天晴自主研发的一款具有全新化学结构的JAK/ROCK抑制剂。正大天晴于2023年欧洲血液学会年会上公布了罗伐昔替尼在慢性移植物抗宿主病(cGVHD)中的Ⅰb/Ⅱ期临床研究数据。结果表明,罗伐昔替尼毒性可耐受,对cGVHD患者各排异器官部位最佳客观缓解率86.7%,40%的患者Lee症状量表(LSS)评分改善≥7分,73.3%的患者降低激素使用剂量,有望为cGVHD患者带来更多的临床治疗选择。另外,正大天晴于今年4月份宣布罗伐昔替尼片用于治疗中高危骨髓纤维化(MF)的关键注册临床研究已达到主要终点,该药用于治疗中高危骨髓纤维化的上市申请也于今年7月份获得国家药监局药品审评中心(CDE)受理。
11月份正大天晴发起的3项Ⅱ期临床试验中,有两项与乙肝相关。进展稍快的一项临床试验(NCT06644417)对象为TQA3605,靶点和作用机制尚未公布。另一项适应证为乙肝的Ⅱ期临床试验(NCT06706310),试验对象为TQA3334,是一种TLR7受体激动剂。
剩余的一项Ⅱ期临床试验(NCT06566586),试验对象为TQB3702,适应证为B细胞淋巴瘤。TQB3702是一种高选择性布鲁顿酪氨酸激酶(BTK)抑制剂。多种B细胞相关恶性肿瘤的发生与BTK的异常活化有关。BTK抑制剂通过抑制BTK的活性,从而起到控制肿瘤生长和转移的作用。
正大天晴发起的3项Ⅰ期临床试验中,有一项(NCT06662773)的招募对象为健康人群,目的在于研究多种药物之间的相互作用,试验对象为库莫西利。库莫西利是一种新型周期蛋白依赖性激酶2、4和6(CDK2/4/6)抑制剂,对CDK2、CDK4、CDK6激酶有不同程度的抑制效果,并且对CDK4激酶具有较强的抑制能力。研究结果显示,库莫西利对CDK2具有抑制作用,其增强的CDK2和CDK4抑制活性可能有助于在临床上克服目前CDK4/6抑制剂的耐药性问题。另外,今年7月,正大天晴自主研发的1类创新药库莫西利胶囊联合氟维司群注射液(商标名:晴可依),已向CDE递交新药上市申请并获受理,用于既往内分泌经治的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性局部晚期或转移性乳腺癌的治疗。
剩余的两项Ⅰ期临床试验中,有一项(NCT06662760)的适应证为晚期肿瘤,试验药物为TQB3002。TQB3002是正大天晴自主开发的口服小分子四代EGFR抑制剂,通过与胞内酪氨酸激酶结合域的ATP位点竞争性结合,抑制相关酪氨酸激酶活性和细胞内磷酸化过程,进而抑制EGFR下游的信号传导,最终导致肿瘤细胞死亡。临床前研究结果显示,TQB3002展现出了出色的抑制活性,能够有效地抑制EGFR单突变(包括EGFRd746-750和EGFRL858R)以及EGFR双突变(如EGFRd746-750/T790M和EGFRL858R/T790M)的激酶活性。这一特性使得TQB3002在针对多种EGFR突变类型的肿瘤治疗中具有潜在优势。
另一项Ⅰ期临床试验(NCT06672276)的药物为TQD3606,适应证为耐药性革兰氏阳性菌、革兰氏阴性菌和厌氧菌治疗。公开资料显示,该产品可能是一个复方制剂,可能含有美罗培南与阿维巴坦。阿维巴坦是一种新型β-内酰胺酶抑制剂,可大幅提高头孢类产品的抗菌活性。美罗培南是一种β-内酰胺类抗生素,用于治疗多种不同的感染,包括脑膜炎及肺炎。
(数据来源于美国Clinicaltrial数据库,统计时间为2024年12月4日)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:张可欣)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐